医薬部外品の申請区分
更新日:2025年3月21日
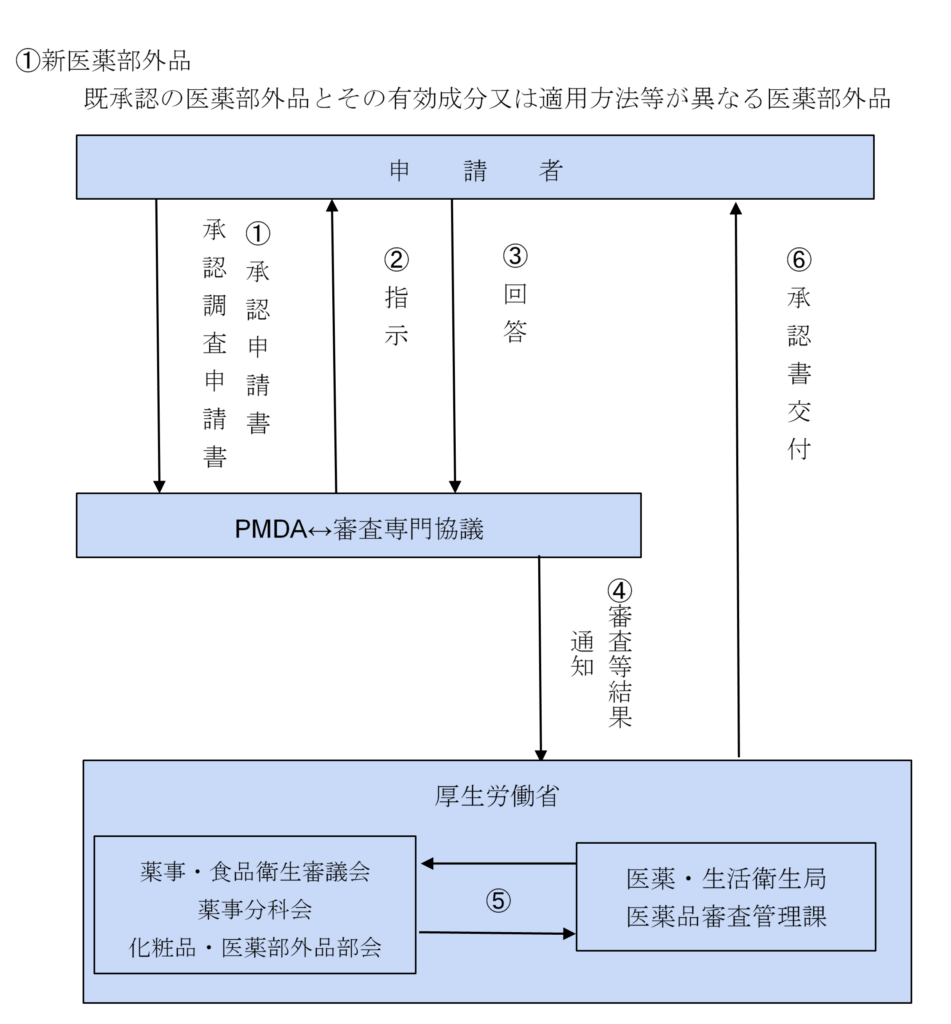
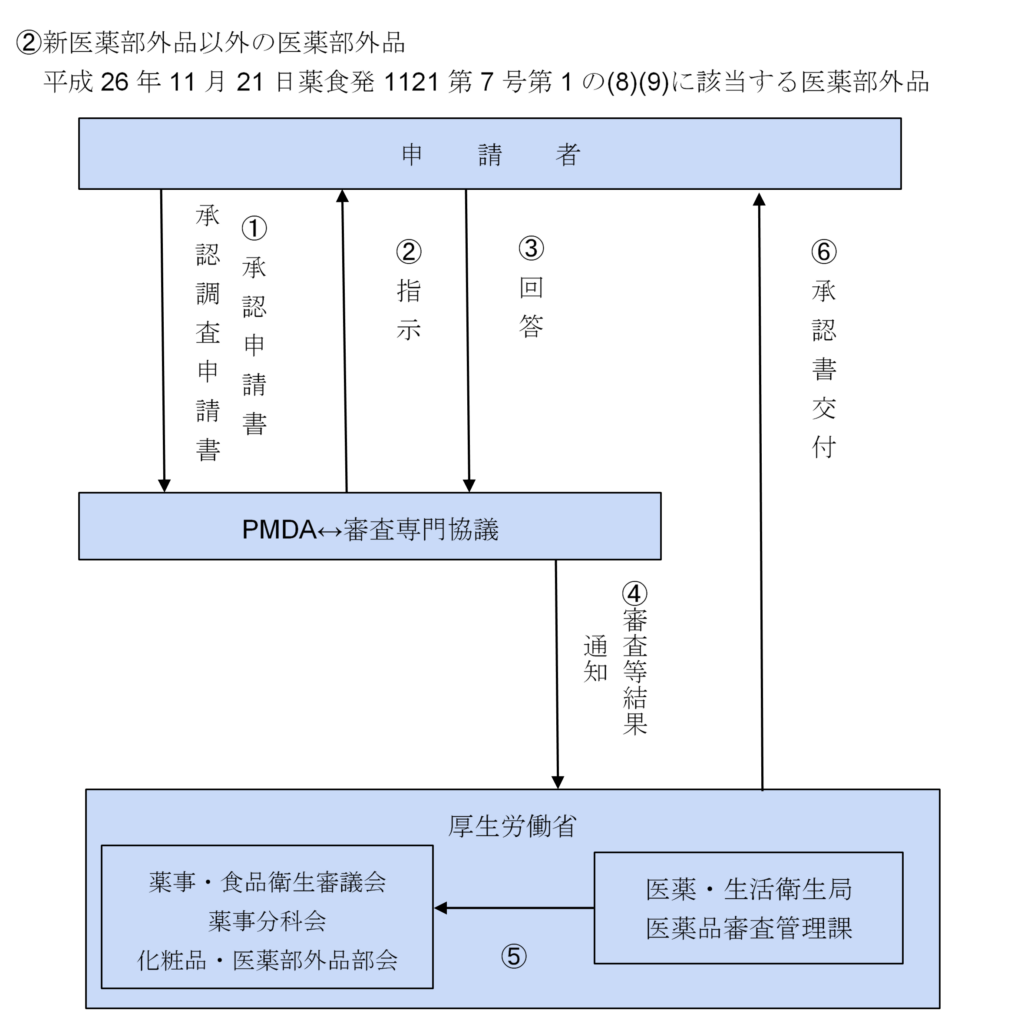
医薬部外品は、医薬部外品は、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(以下「医薬品医療機器等法」と呼ぶ)の規程に基づき、品質、有効性及び安全性等の観点から医薬部外品として適当であるか否かの確認を行い、製品を市場へ出荷又は上市することに対する一般的禁止の解除を行うため、承認申請手続きが必要になります。 配合される成分・分量、効能、効果等により申請区分が分けられており、この区分によって必要とされる添付資料の種類が異なってきますので注意が必要です。
(平成26年11月21日 薬食発1121第7号)
1.医薬部外品の申請区分と定義
| 区分 | 区分名称 | 内容 |
| (1) | 新有効成分含有医薬部外品 | 既承認医薬部外品と有効成分が異なる又は適用方法が明らかに異なる医薬部外品 |
| (2)-1 | 新効能医薬部外品 | 既承認医薬部外品と有効成分は同一であるが、効能・効果が異なる医薬部外品 |
| (2)-2 | 新剤形医薬部外品 | 既承認医薬部外品と有効成分は同一であるが、剤形が異なる医薬部外品 |
| (2)-3 | 新含量医薬部外品 | 既承認医薬部外品と有効成分は同一であるが、配合量が異なる医薬部外品 |
| (2)-4 | 新配合医薬部外品 | 既承認医薬部外品と有効成分及びその配合量は同一であるが、既承認医薬部外品と有効成分の組合せが異なる医薬部外品 |
| (2)-5 | 新用法医薬部外品 | 既承認医薬部外品と有効成分は同一であるが、用法が異なる医薬部外品 |
| (3) | 新添加物含有医薬部外品 | 使用前例のない添加物を配合する又は使用前例のある添加物であっても前例を上回る量を配合する等の医薬部外品 |
| (4) | 類似医薬部外品 | 既承認品目と同一ではないが、新たに有効性、安全性に関する試験を実施しなくても、既承認品目と同一性があるものに相当と判断し得る医薬部外品 |
| (5)-1 | 同一医薬部外品 | 既承認医薬部外品と有効成分及びその配合量、有効成分の組合せ、効能・効果、用法・用量及び剤形が同一の医薬部外品、又は医薬部外品の各種製造販売承認基準に適合する医薬部外品 |
| 区分 | 区分名称 | 内容 |
| ⑸-2 | 新指定医薬部外品 | 医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和35 年法律第145 号)第2条第2項第3号の規定に基づき厚生労働大臣の指定する医薬部外品(平成21 年2月6日付け厚生労働省告示第25 号。以下「指定告示」という。)の(1)、(13)、(15)、(19)、(20)及び(24)に掲げる医薬部外品 |
| (1)胃の不快感を改善することが目的とされている物 | ||
| (13)滋養強壮、虚弱体質の改善及び栄養補給が目的とされている物 | ||
| (15)すり傷、切り傷、さし傷、かき傷、靴ずれ、創傷面等の消毒又は保護に使用されることが目的とされている物 | ||
| (19)肉体疲労時、中高年期等のビタミン又はカルシウムの補給が目的とされている物 | ||
| (20)のどの不快感を改善することが目的とされている物 | ||
| (24)ひび、あかぎれ、あせも、ただれ、うおのめ、たこ、手足のあれ、かさつき等を改善することが目的とされている物 |
| 区分 | 区分名称 | 内容 |
| ⑸-3 | 新範囲医薬部外品 | 指定告示の(2)、(4)から(12)、(14)、(16)、(22)、(23)及び(27)に掲げる医薬部外品 |
| (2)いびき防止薬 | ||
| (4)カルシウムを主たる有効成分とする保健薬(第十九号に掲げるものを除く。) | ||
| (5)含嗽薬 | ||
| (6)健胃薬(第一号及び第二十七号に掲げるものを除く。) | ||
| (7)口腔咽喉薬(第二十号に掲げるものを除く。) | ||
| (8)コンタクトレンズ装着薬 | ||
| (9)殺菌消毒薬(第十五号に掲げるものを除く。) | ||
| (10)しもやけ・あかぎれ用薬(第二十四号に掲げるものを除く。) | ||
| (11)瀉下薬 | ||
| (12)消化薬(第二十七号に掲げるものを除く。) | ||
| (14)生薬を主たる有効成分とする保健薬 | ||
| (16)整腸薬(第二十七号に掲げるものを除く。) | ||
| (22)鼻づまり改善薬(外用剤に限る。) | ||
| (23)ビタミンを含有する保健薬(第十三号及び第十九号に掲げるものを除く。) | ||
| (27)第六号、第十二号又は第十六号に掲げる物のうち、いずれか二以上に該当するもの |

サポート行政書士法人に相談ください。
私どもサポート行政書士法人では、医薬部外品にかかる手続きについて数多く実績があり、専門スタッフがお客様の各種申請を迅速かつ確実に代行しています。
①スピード対応
弊社のスピード対応は多くのお客様から評価いただいており、組織体制の構築から書類作成、
許可取得を経た後の事業開始まで、貴社の1日でも早い参入をサポートします。
②コンタクトしやすい体制
弊社ではご相談は無料で受けています。
弊社は東京・名古屋・大阪の全国3箇所にオフィスを構えており、そこを起点に全国対応しています。
インターネット等を用いて海外からのご相談も承っておりますし、営業時間外でも事前に予約いただければ、夜間や土日祝の相談も可能です。
中国語・英語・韓国語対応のスタッフもいますので、日本語では相談が難しい場合でも対応が可能です。
医薬部外品許可申請のことでお困りの方はどんなことでもぜひ私たちに相談ください!
③コンプライアンス体制構築もしっかりサポート
手順書(GVP、GQP)等について、基準を満たしつつも貴社の実態に合う形で作成することが可能です。
許可の更新の経験も豊富にあり、内部監査のサポートも提供しています。
事業者様にとって許可取得はゴールではなくスタートです。
先を見据えたサポートをしっかりと提供します。

専任スタッフが全国の案件を対応しています。