제조판매업 QMS체제 구축
更新日:2024年10月27日
제조판매업 QMS 구축
의료기기 등의 제조관리 및 품질관리 기준에 대한 적합성 조사는 이전의 제조소별 조사에서 제품에 관한 제조판매업자와 모든 등록제조소를 포함한 품질관리 감독 시스템별로 조사를 실시하는 새로운 규제체계로 변경되었습니다.
이 변경에 따라 ‘의료기기 및 체외진단용 의약품의 제조관리 및 품질관리 기준에 관한 성령'(약칭:QMS 성령)이 개정되어 새롭게 제조판매업에 대해서도 적용되게 되었습니다.
의료기기 등의 제조판매업 허가요건을 재검토하여 GQP 성령 대신 QMS 체제 성령에 적합하다는 것이 요건 중 하나입니다.
또한 제품과 관련된 품질관리 감독시스템 전체를 조사하기 위해 이전에 실시되었던 도도부현 조사는 폐지되고 승인품목은 PMDA가, 인증품목은 등록인증기관이 각각 조사를 실시합니다.
단, 의료기기 등의 제조관리 및 품질관리 상황을 확인하기 위한 출입검사 등은 이어서 원칙적으로 광역자치단체가 실시하게 되어 있습니다.
| 조항 | QMS 성령 |
| 품질방침 표명 | 제6조 제1항 제1호 |
| 품질목표 표명 | 제6조 제1항 제1호 |
| 품질관리 감독시스템 기준서 | 제6조 제1항 |
| 절차를 규정하는 문서 | 제6조 제1항 제4호 |
| 약사에 관한 법령 규정에 따라 문서화하도록 요구되는 사항 | 제6조 제1항 제5호 |
| 제품표준서 | 제6조 제2항 |
| 업무에 종사하는 부문 및 구성원의 책임 및 권한 | 제15조 제1항 |
| 업무 운영 기반의 보수 관련 요구사항 | 제24조 제2항 |
| 구성원의 건강상태, 청정의 정도 등에 관한 요구사항 | 제25조 제2항 |
| 작업환경 조건 관련 요구사항 | 제25조 제3항 |
| 오염된 제품 등의 관리에 관한 실시 요령 | 제25조 제5항 |
| 제품의 리스크 관리에 관한 요구사항 | 제26조 제5항 |
| 제품요구사항과 관련된 문서 | 제28조 제2항 |
| 설계개발계획 관련 문서 | 제30조 제5항 |
| 구매정보가 기재된 문서 | 제38조 제3항 |
| 제조 및 서비스 제공에 관한 요구사항 | 제40조 제1항 |
| 제조 및 서비스 제공에 관한 작업지도서 | 제40조 제1항 |
| 제품의 청정에 관한 요구사항 | 제41조 |
| 설치업무 관련 요구사항 | 제42조 제1항 |
| 부대서비스업무 실시 등에 관한 작업지도 관련 체계 | 제43조 제1항 |
| 제품 유지에 관한 작업 지시에 관한 체계 | 제52조 제1항 |
| 사용 기한이 한정된 제품 등의 관리와 관련된 작업지도 관련 체계 | 제52조 제2항 |
| 제조 재시도에 관한 절차 | 제60조 제9항 |
| 제조 재시도에 관한 악영향 | 제60조 제10항 |
| 통지서 | 제62조 제2항 |
| 품질관리 감독 시스템을 문서화한 것 | 제66조 |
| 모든 시설 및 관련 등록 제조소에 대하여 해당 시설 등이 제품에 관하여 시행규칙 제228조의20제2항 각 호에 열거된 사항을 안 경우에 해당 사항을 해당 제조판매업자 등에게 통지하게 하기 위한 절차 | 제69항 |
| 국내 품질업무 운영책임자의 업무를 규정한 문서 | 제72조 제2항 |
| 제조판매업자와 관련된 시설 및 등록제조소 간의 결정 | 제72조의2 |
| 수리업자로부터의 통지 처리에 관한 절차 | 제72조의2제2항 제1호 |
| 판매업자 또는 대여업자의 품질 확보에 관한 절차 | 제72조의2제2항 제2호 |
| 중고 판매업자 또는 대여업자로부터의 통지 처리에 관한 절차 | 제72조의2제2항 제3호 |
QMS 성령에 의해 절차서화가 요구되는 조항
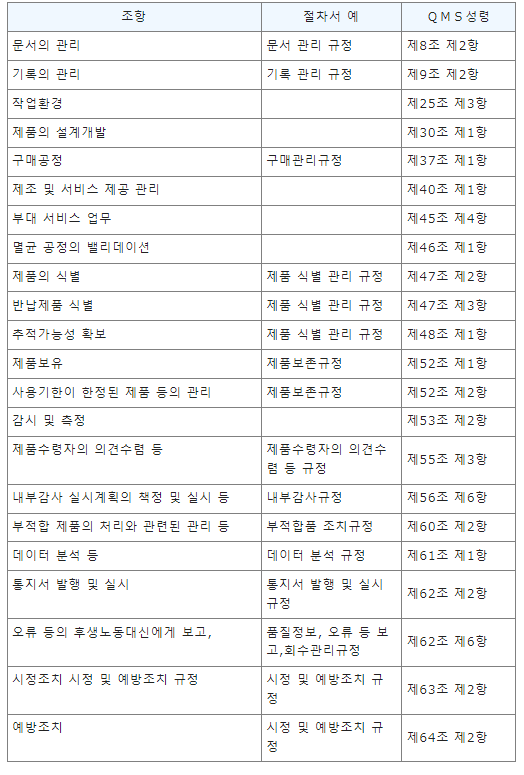
QMS 성령에 의해 기록이 요구되는 조항
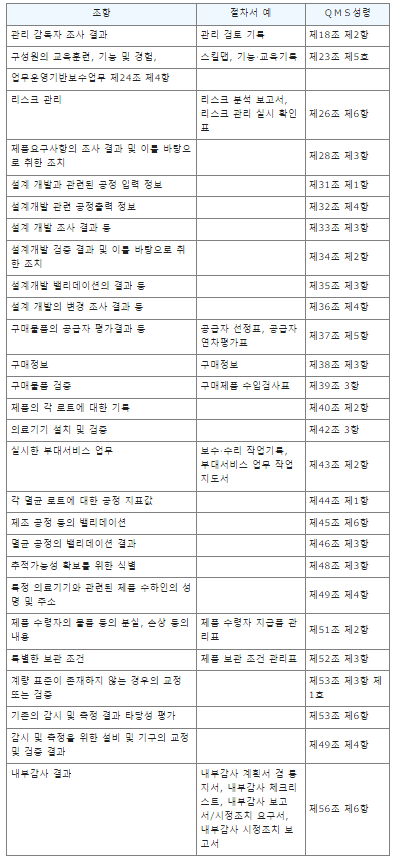
관련 통지 모음
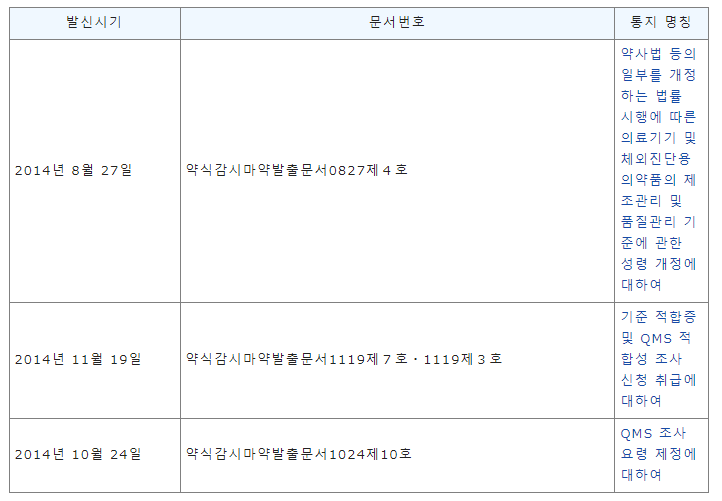
의료기기에 관한 인허가 상담은 지원행정서사 법인으로
서포트행정서사법인에서는 신규로 의료기기 업계에 참가하시는분부터 기존의 제조판매업자, 제조업자, 판매업자 여러분께 의약품 의료기기 등 법에 관한 신청지원 및 컨설팅을 실시하고 있습니다.