体外診断用医薬品を製造販売する
体外診断用医薬品を製造販売する
体外診断用医薬品を製造販売する場合には、製造販売業許可が必要です。また、許可の有効期限(5年)を超えて引き続き製造販売しようとする場合には、許可の更新が必要です。
なお、この許可のみでは製品を製造することはできません。
自社において国内で製造して市場に出荷するには、製造販売業許可と製造業登録の両方が必要となります。
また、製造販売業許可と製造業登録の後に製品ごとの承認、認証、届出等の手続きが必要となります
(製造業登録は下記参照)。 製造販売業許可は各都道府県に申請となりますが、自治体によって多少提出するものが変わります。各都道府県の窓口に提出し知事により許可されます。
体外診断用医薬品の場合、製造販売業では総括製造販売責任者が薬剤師でなければなりません。
人的要件にご注意ください。
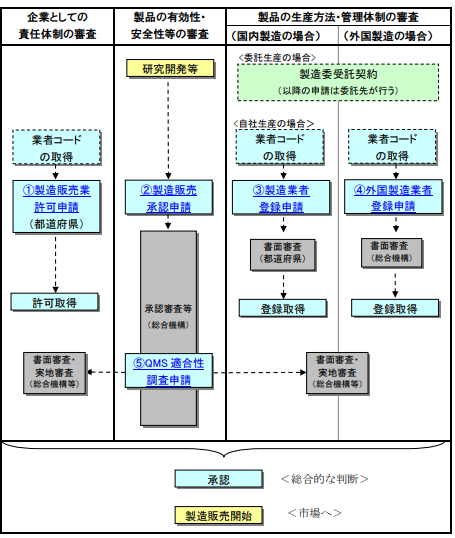
製造販売の流れ
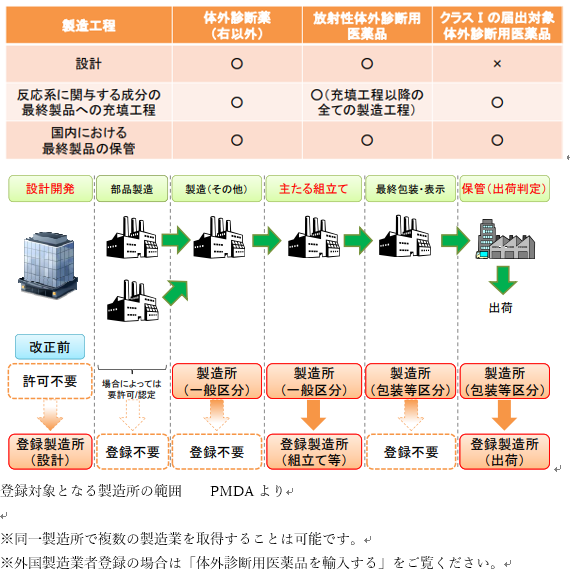
体外診断用医薬品を製造する(国内:製造業者登録)
体外診断用医薬品の製造をする場合には、製造所(体外診断用医薬品の製造工程のうち設計、組立て、包装その他の厚生労働省令で定めるものをするものに限る。)ごとに、製造業登録が必要です。
また、登録の有効期間(5年)を超えて引き続き製造しようとする場合には、登録の更新が必要です。
この登録のみでは市場への出荷は出来ません。
各都道府県の窓口に提出し知事により登録されます。こちらは各都道府県に申請となりますが自治体によって多少提出するものが変わります。 製造業では責任技術者製造管理者が薬剤師でなければなりません。
人的要件にご注意ください。
体外診断用医薬品の品目手続き
個々の体外診断用医薬品を市場へ流通させるためには、上記の許可・登録を受けたうえで体外診断用医薬品ごとに承認の手続を行わなければなりません。
体外診断用医薬品の製造管理、品質管理の基準に適合していることを総合機構等へ申請しQMS適合性の実地調査を受ける必要があります。
体外診断用医薬品に関する許認可のご相談はサポート行政書士法人へ
サポート行政書士法人では、新規で体外診断用医薬品業界へ参入される方から、既存の製造販売業者・製造業者・販売業者の皆さまに対して、申請サポートやコンサルティングを行っています。
体外診断用医薬品の申請は専門性が高く、対応している行政書士が少ない分野の一つと言えます。
日々企業の皆様の代理人として行政庁への申請や折衝を行っている行政書士だからこそ蓄積できるノウハウ・実績を元に、体外診断用医薬品に関する法務サービスを提供いたします。
弊社の担当者は、全国の都道府県で申請実績があります。ぜひご相談ください。